|
|
|

|
|
|
防今秋Omicron再變種 FDA擬升級補強劑
|
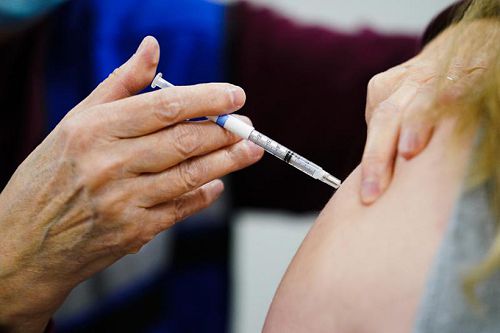 FDA建議秋季施打次世代疫苗。 FDA建議秋季施打次世代疫苗。
|
|
|
(華盛頓二十八日電)Omicron亞型變異株BA.4及BA.5加速在美國傳播,美國疾病防治中心(CDC)周二(28日)表示,截至本月25日,全美新冠確診病例當中,估計約有52%是感染BA.4與BA.5。在此同時,美國食品藥物管理局(FDA)專家小組則建議,今年秋季要開始推動施打能防範新型變種病毒的次世代疫苗當做加強劑。
截至6月18日,BA.4和BA.5病例約佔美國確診者3分之1,短短一周內增加為全美病例的半數。根據CDC估計,從6月19日至6月25日之間,美國確診者中約有15.7%是感染BA.4,36.6%是感染BA.5。截至6月25日,美國確診病例的7日移動平均數是10萬1378例,比前一周增加2.9%。
世界衛生組織已在3月間把BA.4與BA.5納入監察名單,歐洲疾病防治中心(ECDC)也把這兩種病株列為高關注變異株。在此同時,美國FDA的疫苗專家小組28日開會,以19票比2票通過建議下一波推動的疫苗加強劑要納入能對抗Omicron變異株的次世代疫苗,專家認為疫苗應要能防範BA.4與BA.5,FDA預定7月初對疫苗定案。
FDA生物製劑評估研究中心主任馬克斯(Peter Marks)表示,他們希望能在今年10月前推動施打新疫苗當做加強劑,新的疫苗需要更能防範目前流行的病株,防護效果更好,保護力更持久。
輝瑞(Pfizer Inc),莫德納(Moderna Inc)和諾瓦瓦克斯(Novavax Inc)3家疫苗製造業者都在FDA這場專家會議提供最新研究數據,3家業者均針對Omicron BA.1病株研發了改良疫苗,並進行實驗。
莫德納表示,可防範BA.1的疫苗,可望於9月量產,如要針對新的亞型變異株改良,估計要等到10月底或11月初。
輝瑞和合作夥伴BNT則表示,已準備好大量針對BA.1的疫苗,也準備針對BA.4與BA.5改良疫苗,預計10月初可量產。
莫德納和輝瑞均宣稱,他們針對BA.1研發的次世代疫苗均能對Omicron產生不錯的免疫反應,也能對抗BA.4與BA.5,只是保護力不像對抗BA.1那麼強。
|
|
|
[Back]
|
|
|